
Les principaux protagonistes
L'électron
L'électron est un corpuscule extrêmement léger, considéré comme un des constituants fondamentaux de la matière. Porteur d'une charge électrique élémentaire, il circule autour du noyau de l'atome. Certains noyaux, radioactifs b- (bêta-moins), expulsent des électrons.

Le proton
Le proton est, avec le neutron, l'un des constituants du noyau de l'atome. Il constitue le noyau de l'atome d'hydrogène. Porteur d'une charge électrique élémentaire positive et 1836 fois plus lourd que l'électron, c'est une particule petite, mais complexe, sensible aux forces nucléaires. Le nombre de protons dans le noyau est égal au nombre d'électrons de l'atome.

Le neutron
Le neutron est, avec le proton, l'un des constituants du noyau de l'atome. Il en est le partenaire. Il est instable en dehors du noyau. Dénué de charge électrique, il n'est sensible qu'aux forces nucléaires. Étant électriquement neutre, il est facilement capté dans le noyau, y déclenchant des réactions nucléaires.

Le nucléons
On appelle nucléons, du mot latin nucléus qui signifie noyau, les protons et les neutrons qui composent le noyau de l'atome. Les deux espèces de nucléons y jouent un rôle très similaire : ils possèdent une masse très voisine et ne sont distingués que par leur charge électrique.

L'électron positif ou positon
Le positon ou électron positif est défini comme l'antiparticule de l'électron. Sa masse et sa façon d'agir en traversant la matière sont les mêmes. Comme son nom l'indique, il est porteur d'une charge électrique (élémentaire) positive. Certains noyaux, radioactifs b+ (bêta-plus), excédentaires en protons, expulsent des positons. Particule d'antimatière, perdue dans un univers de matière, un positon b disparaît rapidement en s'annihilant avec un électron pour produire deux photons.

Le neutrino et l'antineutrino
Le neutrino apparaît comme le partenaire de l'électron, de la même façon que le neutron est le partenaire du proton dans le noyau. Corpuscule élémentaire, dépourvu de charge électrique, de masse pratiquement nulle, le neutrino interagit extrêmement peu avec la matière. Dans les désintégrations b des noyaux, il se manifeste comme une particule invisible qui emporte avec elle une partie de l'énergie disponible. Tout aussi invisible, l'antineutrino, antiparticule du neutrino, est le partenaire du positon.

Les isotopes
On appelle isotopes, des noyaux qui diffèrent par le nombre de neutrons. Des isotopes possèdent les mêmes propriétés chimiques et atomiques. Par contre les propriétés nucléaires sont différentes, car le nombre de neutrons influe sur la stabilité du noyau. La majorité des atomes présents dans la nature sont des isotopes stables. Les isotopes radioactifs, beaucoup plus nombreux, ont généralement disparu en raison de leur instabilité. Ils peuvent être recréés artificiellement par exemple pour des applications médicales.

Les rayons alpha


Les rayons bêta
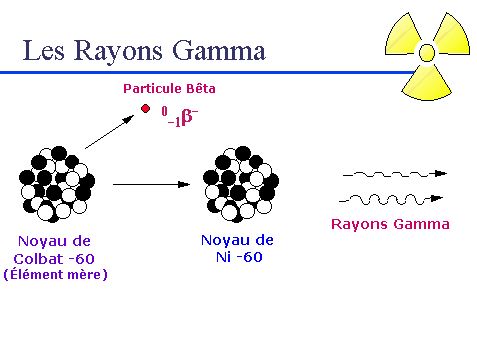
On appelle électrons "bêta" les électrons émis spontanément par certains noyaux radioactifs excédentaires en neutrons : c'est la radioactivité bêta-moins (b-) appelée ainsi parce que la charge électrique de l'électron est négative. Des noyaux excédentaires en protons émettent en sens inverse des anti-électrons ou positons bêta : c'est la radioactivité bêta-plus (b+) qui est beaucoup plus rare dans la Nature.


Les rayons gamma

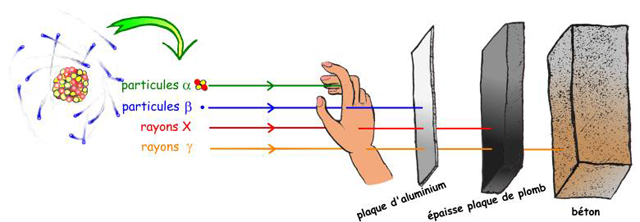
La pénétration des rayons


Les unités
Unités d'énergie : eV, keV, MeV
L'unité d'énergie adaptée à l'échelle de l'atome est une quantité appelée l'électronvolt ou eV. L'énergie nécessaire pour arracher un des électrons externes d'un atome, ou l'énergie libérée lors d'une réaction chimique, est de quelques eV. L'électronvolt est une unité très petite (0,16 milliardième de milliardième de joule). Les énergies mises en jeu dans le noyau sont environ un million de fois supérieures à celles observées dans les phénomènes chimiques. Pour cette raison, il est commode d'exprimer les énergies nucléaires en millions d'électronvolts ou MeV. L'unité intermédiaire est le millier d'électronvolts ou keV.

Unités d'activité, becquerel, curie
Le becquerel ou Bq est l'unité d'activité. Un becquerel équivaut à une désintégration par seconde. C'est une unité extrêmement petite. Le becquerel remplace une unité historique longtemps employée, le curie ou Ci. Un curie vaut 37 milliards de becquerels. C'est l'activité d'un gramme de radium.

Le gray : unité de dose de dépôt d'énergie
L'unité de dose de dépôt d'énergie par les rayonnements radioactifs est le gray (Gy). Un gray correspond à un dépôt d'énergie d'origine radioactive d'un joule par kilogramme de matière. Contrairement au sievert, le gray ne distingue pas si le dépôt a lieu dans la matière inerte ou dans la matière vivante. Cependant, pour des expositions importantes ou courtes, les doses exprimées en gray sont plus significatives que les doses exprimées en sievert.

Le sievert : unité de dose biologique
L'unité de dose d'irradiation significative pour un être vivant est le sievert ou Sv. Comme cette unité est assez grande, on exprime beaucoup plus souvent les doses biologiques en millisievert ou mSv. En Europe, la dose annuelle moyenne à laquelle la population est exposée est environ de 4 mSv par personne.

Tableau récapitulatif
|
Mesure
|
Unité
|
Ce qui est mesuré
|
Valeur
|
Exposition
|
Roentgen (R)
Coulombs/kg
|
Mesure l'exposition aux rayonnement X ou gamma.
|
1 R = 2.58 x 10-4 Cb/kg
|
Dose Absorbée
|
Rad
Gray (Gy)
|
Mesure la dose absorbée de rayonnements ionisant.
|
1 rad = 100 ergs*/gram
1 Gy = 100 rad
|
Dose biologique
|
Rem
Sievert (Sv)
|
Mesure la capacité de la dose de radiation absorbée à causer des dégats biologiques.
|
Rem = rad x Facteur de Qualité
1 Sv = 100 rem
|
* Un erg est une unité de travail.
Les coulombs/kilogramme, le Gray et le Sievert sont des unités du Système International (S.I.).
1 curie (Ci) = 3.7 x1010 Désintégrations par seconde (dps)
1 Becquerel (Bq) = 1 désintégration par seconde (dps).


Divers
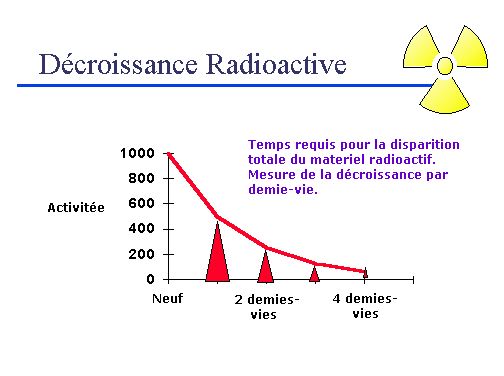
La période
La " période " ou " demi-vie " d'un élément radioactif est le temps nécessaire pour que sa radioactivité diminue de moitié. Ce temps caractéristique ne dépend pas de l'âge de l'échantillon. La radioactivité décroÎt très vite avec le nombre de périodes : elle est divisée par 1000 au bout de dix périodes. Pour les déchets radioactifs, on parle de " vie courte " lorsque la période est inférieure à 5 ans et de " vie moyenne " lorsqu'elle est comprise entre 5 et 100 ans ; les noyaux dont la période dépasse 100 ans sont dits " à vie longue ". Les isotopes utilisés pour les diagnostics médicaux sont à vie très courte.

La période biologique
La période biologique mesure le temps qu'un atome absorbé (hydrogène, carbone, oxygène, calcium, etc.) passe dans le corps humain. Plus la période biologique est courte, moins un élément radioactif ingéré a de chances de se désintégrer durant son séjour dans l'organisme, et moins il est dangereux.

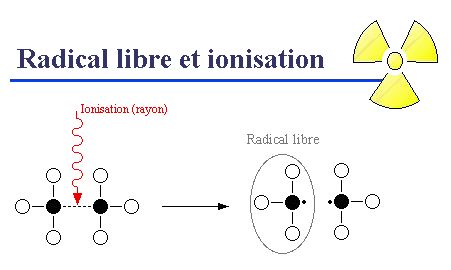
Ionisation
Les particules électriquement chargées ont la faculté d'arracher des électrons appartenant aux atomes de la matière qu'elles traversent. Ce phénomène est appelé ionisation, car les atomes qui ont perdu des électrons sont devenus des ions. En ionisant, les particules chargées perdent de leur énergie et se ralentissent. Les particules alpha et bêta sont capables d'ioniser des centaines de milliers d'atomes le long de leur parcours.

La fission
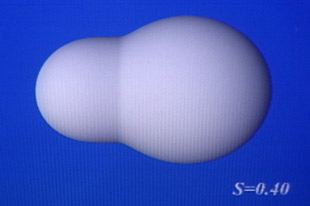
La fission est la fragmentation d'un noyau en deux morceaux. La fission se produit exceptionnellement de manière spontanée. Cette désintégration provoquée est en réalité une réaction nucléaire. La fission serait restée un phénomène marginal s'il n'était possible de la multiplier à travers un mécanisme de réaction en chaîne. La réaction en chaîne peut prendre un tour explosif (bombe atomique) ou être contrôlée (réacteurs nucléaires). La fission met à la disposition de l'humanité une forme d'énergie pratiquement inépuisable. Elle produit des corps radioactifs, les déchets nucléaires.

Les produits de fission
On appelle produits de fission les noyaux produits par la fragmentation d'un noyau fissile. Immédiatement après la fission, ces fragments sont beaucoup trop riches en neutrons pour être stables. Très radioactifs, ils cherchent à retrouver la stabilité par une suite de désintégrations. Le retour à la stabilité prend un temps très variable. Les produits de fission constituent l'essentiel, avec les actinides, des déchets radioactifs que l'on retrouve lors de la décharge du combustible des réacteurs nucléaires. Dominants au départ, ils disparaissent plus rapidement que les actinides.

Les actinides
Les captures de neutrons dans le combustible des réacteurs nucléaires, ne provoquent pas toujours des fissions. Elles contribuent également à produire des noyaux plus lourds que l'uranium, appelés actinides. L'actinide le plus connu est le plutonium-239, qui est fissile. Les actinides (principalement des isotopes du neptunium, du plutonium, de l'américium et du curium) sont des noyaux instables, mais à durée de vie plus longue en général que les produits de fission. Leur relative abondance et ces durées de vie posent un problème pour le stockage des déchets radioactifs en provenance des réacteurs.

Les rayons cosmiques
Le soleil est un gigantesque réacteur nucléaire autour duquel la planète Terre gravite avec obstination depuis près de cinq milliards d'années. Contrairement aux réacteurs nucléaires inventés et crées par l'homme, ce réacteur n'est pas " protégé "; c'est à dire que les réactions nucléaires qui s'y produisent émettent des rayonnements particulaires et électromagnétiques que rien ne peut arrêter ou atténuer puisque le soleil évolue dans le vide. Fort heureusement pour notre survie, seule une partie des rayonnements émis par le soleil atteint la surface de la Terre.

Le "vent" solaire
C'est une expression qui désigne de façon générique les particules émises par le soleil qui viennent heurter la Terre et les autres corps constituant le système solaire.

La convection naturelle
C'est le mouvement d'un fluide avec transport de chaleur, sous l'influence de différences de température.

Une chaîne trophique
C'est la hiérarchie relative à la nutrition de l'ensemble des êtres vivants.


